¿Qué es el Trasplante de Médula ósea o Trasplante de progenitores Hematopoyéticos?
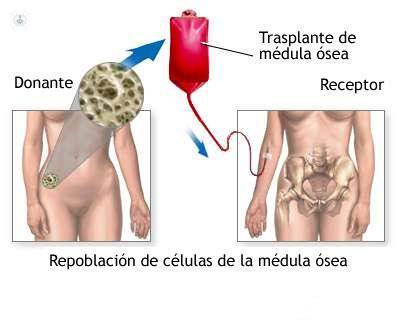
El trasplante de precursores hematopoyéticos, más conocido como trasplante de médula ósea, es el tratamiento mediante el cual se destruye la Médula ósea de un paciente, reemplazándola por precursores hematopoyéticos nuevos. Suele realizarse en pacientes con cáncer o enfermedad congénita de la sangre o de médula ósea. El objetivo es eliminar las células enfermas o defectuosas e introducir células madre que produzcan células sanguíneas sanas.
Origen del trasplante de médula ósea
El primer trasplante de médula ósea fue realizado por Georges Mathé, un oncólogo francés, en 1958, para intentar salvar la vida de seis investigadores nucleares que habían sido sometidos a radiaciones por accidente en el Vinca Nuclear Institute. Aunque todos los pacientes sufrieron rechazo al trasplante, Mathé comprendió la necesidad de mejorar el procedimiento, de gran potencial dentro del campo de la inmunoterapia.
Tras años de investigación, Mathé logró mejorar la técnica, convirtiéndose en el pionero del uso de trasplante de médula ósea en el tratamiento contra la leucemia. El trasplante fue realizado usando derivados de células madre de médula ósea por un equipo en el Centro de Investigación de Cáncer Fred Hutchinson de 1950 a 1970 por E. Donnall Thomas, cuyo trabajo fue reconocido posteriormente con el premio Nobel de Medicina.
Para qué se utiliza el trasplante de médula ósea
El Trasplante de médula ósea ó de progenitores hematopoyéticos purificados se usa para tratar diversos tipos de enfermedades:
- Aplasia de médula ósea
- Enfermedades hereditarias
- Leucemia
- Linfoma
- Inmunodeficiencias
Muchos receptores son pacientes de mieloma múltiple o de leucemia, quienes no se podrían beneficiar de un tratamiento citostático prolongado, o que ya tienen resistencia a la quimioterapia. Son también candidatos aquellos casos pediátricos donde el paciente tiene defecto congénito medular grave, como la neutropenia congénita o inmunodeficiencia combinada, con células madre defectuosas, y también niños o adultos con anemia aplásica, quienes han perdido sus células madre en el momento del nacimiento.
Otras enfermedades tratadas con trasplantes de médula ósea incluyen: anemia falciforme, síndrome mielodisplásico, neuroblastoma, linfoma, Sarcoma de Ewing, tumor desmoplásico de células pequeñas y redondas, enfermedad granulomatosa crónica o enfermedad de Hodgkin.
Asimismo, recientemente el trasplante no mieloblativo o “trasplante mini” ha desarrollado procedimientos que requieren menos dosis de quimioterapia preparativa y radiación. Esto ha permitido extender la terapia a pacientes más mayores, junto con otros enfermos, considerados demasiado débiles para mantener un tratamiento tan agresivo.
Tipos de trasplante de progenitores hematopoyéticos o médula ósea
Después de varias semanas de crecimiento en la médula ósea, la expansión de las células madre hematopoyéticas y su progenie es suficiente para normalizar los recuentos de células sanguíneas y reiniciar el sistema inmunológico.
Según el origen de las células madre, conocemos los siguientes:
1) Autólogo
Este tipo de procedimiento usa precursores hematopoyéticos del mismo paciente que va a recibir el trasplante. Como las células trasplantadas se toman de la médula ya dañada, muchos protocolos emplean algunas técnicas para escoger las células sanas que se van a devolver al paciente. Este proceso puede requerir medicamentos o anticuerpos diseñados para eliminar ciertos tipos de células o purgar la médula de células neoplásicas.
Para realizar esta terapia se requiere la extracción (aféresis) de células madre hematopoyéticas del paciente y almacenar las células recolectadas en un congelador. Después el paciente es tratado con altas dosis de quimioterapia con o sin radioterapia, con la intención de erradicar las células malignas, teniendo como consecuencia la ablación total o parcial de la médula ósea (destrucción de la capacidad de la producción de nuevas células de la médula ósea). Posteriormente los progenitores hematopoyéticos sanos se devuelven al torrente sanguíneo del paciente, remplazando el tejido destruido y reanudando la producción normal todas las series hematológicas.
Un trasplante autólogo tiene la ventaja de tener un riesgo menor de padecer alguna infección durante la parte inmunocomprometida del tratamiento, ya que la recuperación de la función inmune es rápida. Además, la incidencia de pacientes que experimentan rechazo es muy raro, debido a que la donación y recepción es del mismo individuo. Estas ventajas han hecho considerar por parte de los expertos en Hematología el trasplante autólogo como tratamiento estándar para enfermedades como linfomas. Sin embargo, para otras como la leucemia mieloide aguda, el aumento de la probabilidad de recaída hace que la modalidad alogénica sea la elegida.
2) Alogénico
Este tipo de trasplante usa precursores hematopoyéticos tomados de un donante distinto al receptor. Este trasplante tiene, a su vez, distintas variedades, según el donante y la similitud del sistema de Antígenos Leucocitarios Humanos (HLA). Es importante reconocer de qué tipo de trasplante se habla, ya que tanto la utilidad como los resultados varían de uno a otros. Cuando el donante es un hermano gemelo univitelino se denomina trasplante singénico. Sin embargo, cuando el donante es un hermano HLA se denomina trasplante alogénico de hermano HLA idéntico. En el caso de que el donante sea un familiar que comparte un solo haplotipo del sistema HLA se denomina trasplante haploidéntico, pudiendo ser un familiar cualquiera (padre, madre, hermanos, primos) que comparte solo la mitad de los genes implicados en el sistema HLA. Si el donante es un donante no emparentado se denomina trasplante de donante no emparentado.
Los trasplantes que involucran a un donante y un receptor no genéticamente idénticos siempre están asociados con diferencias HLA entre injerto y huésped. En estos casos, el sistema inmune trasplantado reconoce como extraños los antígenos del HLA de las células del receptor y las ataca. Por eso es necesario seleccionar donantes maximizando la cantidad de antígenos HLA compartidos por donante y el receptor. Los antígenos HLA son heredados en una manera mendeliana, así que con frecuencia se encuentra un familiar que comparte los genes HLA. Si no hay un donante compatible emparentado se puede buscar un donante no relacionado que sí sea HLA compatible.
Los trasplantes alogénicos también se realizan utilizando sangre del cordón umbilical como fuente de células madre. En general, mediante el trasplante de células madre sanas del sistema inmunitario del receptor, los trasplantes alogénicos de células madre hematopoyéticas parecen incrementar las posibilidades de curación o remisión a largo plazo.
Fuente de los Progenitores hematopoyéticos
- Médula ósea
La médula ósea fue la primera fuente de células madre trasplantadas. Como ya se ha mencionado, este tipo de trasplante se hace con células tomadas directamente de la médula ósea del donante, generalmente aspiradas de las crestas iliacas a través de una aguja de gran tamaño que llega hasta el centro del hueso. La técnica se realiza bajo anestesia general.
- Sangre periférica
Se pueden recolectar células hematopoyéticas de la sangre del donante usando un proceso llamado aféresis. Antes del trasplante, el donante se estimula por inyecciones de Factor estimulante de colonias de granulocitos (G-CSF) para producir y movilizar más precursores hematopoyéticos. La obtención o recolección del donante se realiza mediante una aguja puesta en una vena del brazo conectada a una máquina, que recolecta las células que se van a trasplantar. El resto de sangre se devuelve al donante.
- Sangre del cordón umbilical
La sangre del cordón umbilical contiene células madre que pueden ser trasplantadas después de separación celular hematopoyético del resto del tejido (CD34+ o Lin-). Los trasplantes con sangre del cordón umbilical no requieren tanta compatibilidad entre donante y el receptor. Sin embargo, la cantidad baja de células disponibles en cada cordón hace que el uso de un solo donante para trasplantar en un adulto o joven sea difícil. A veces se usa sangre de cordón umbilical de dos donantes distintos para que el número de células trasplantadas sea suficiente.
Se obtiene cuando una madre dona de su bebé el cordón umbilical y la placenta después del nacimiento. La sangre del cordón tiene mayor concentración de progenitores hematopoyéticos que los que se hallan circulando en la sangre de una persona adulta. Sin embargo, la pequeña cantidad de sangre procedente de un cordón umbilical (normalmente 50 ml) hace que sea más adecuado para el trasplante en niños pequeños que en los adultos. Las nuevas técnicas que utilizan la expansión ex–vivo de unidades de sangre del cordón umbilical o el uso de dos unidades de sangre de cordón de diferentes donantes, permiten que este tipo de trasplante pueda ser utilizado en adultos.
- Acondicionamiento
En la mayoría de los casos se necesita eliminar los progenitores ya presentes en la médula ósea del receptor. Durante este proceso, llamado acondicionamiento, se usan dosis altas de quimioterapia y/o radioterapia para destruir toda la médula ósea del paciente, con el fin de eliminar células cancerosas, evitar el rechazo del injerto, y dejar espacio para el injerto. Regímenes comunes incluyen algunos fármacos.
El acondicionamiento deja al paciente sin sistema inmune e incapaz de producir glóbulos rojos, por lo que moriría si no se le trasplantase una nueva médula. Las terapias tóxicas que se usan en este proceso pueden dañar una variedad de tejidos y son asociadas con complicaciones como trastornos pulmonares y neurológicos y un riesgo más alto de cáncer en el futuro.
En inmunodeficiencias severas, el sistema inmune del receptor ya es bastante débil como para que el trasplante se pueda realizar sin preparación.
- Prendimiento
Inmediatamente después del trasplante, las células madre trasplantadas se alojan en los huesos y empiezan a reconstituir los tejidos hematopoyéticos del paciente. Este proceso, conocido como prendimiento, se lleva a cabo durante unas semanas (generalmente entre el día 15 y 21) tras el tras el implante. El rechazo del injerto puede impedir el prendimiento y dejar al paciente sin función hematopoyética suficiente.
